| 1. |
เลือกวัฏภาคนิ่ง (stationary phase) และวัฏภาคเคลื่อนที่ (mobile phase) สำหรับการแยกให้เหมาะสม (selecting the tools)
ซึ่งโดยทั่วไป คอลัมน์ที่เป็น C18 reverse phase ชนิด silica end caped (type B) จะสามารถแยกสารโดยทั่วไปได้ดีอยู่แล้ว และควรใช้ mobile phase เป็น น้ำกับ acetonitrile (เนื่องจาก acetonitrile มีค่าการดูดกลืนแสงยูวี และ มีความหนืดต่ำทำให้ สามารถวัดค่าการดูดกลืนแสงที่ความยาวคลื่นต่ำถึง 220 nm ได้) หรือ น้ำ กับบัฟเฟอร์ที่พีเอชค่อนข้างเป็นกรด เพื่อลดการแตกตัวของ silanol group ของ stationary phase ดังรายละเอียดในตารางที่ 1
ตารางที่ 1 Recommended starting conditions for reverse-phase LC method development |
| |
Separation variable |
Preferred Initial Choice |
Column |
|
Dimensions |
150 mm x 4.6 mm |
Particle size |
5 ?m |
Stationary phase |
C8 or C18 |
Mobile phase |
|
Solvents A-B |
Water-acetonitrile (for neutral samples) |
%B solvent |
Variable |
Buffer |
25 mM phosphate buffer pH 2.5 or 0.1% trifluoroacetic acid or formic acid (for ionizable samples) |
Additives such as ion-pair reagents and amine |
As necessary |
Flow rate |
1-2 mL/min |
Temperature |
35 oC |
|
| |
|
| 2. |
ทราบถึงปัจจัยที่มีผลต่อประสิทธิภาพการแยก (measuring satisfaction)
สมการที่บอกถึงประสิทธิภาพการแยก คือ สมการการแยกชัด (resolution: Rs) |
| |
|
| |
จากสมการที่ 1 จะพบว่าปัจจัยที่มีผลต่อประสิทธิภาพการแยก จะแบ่งเป็น 3 พจน์ (term) คือ
พจน์ i คือ จำนวนเพลต (plate number: N) จะบอกถึงคุณภาพของคอลัมน์ โดยคอลัมน์ที่มีค่า N มาก (เพิ่มความยาวคอลัมน์) ก็จะทำให้การแยกดีขึ้น แต่ก็จะดีขึ้นแค่เพียงแค่ 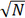 เท่านั้น และยังมีผลให้ความดันเพิ่มมากขึ้นด้วย เท่านั้น และยังมีผลให้ความดันเพิ่มมากขึ้นด้วย
พจน์ ii คือ สมรรถนะการเลือก (selectivity) หรือความสามารถของคอลัมน์และ mobile phase ที่มีผลต่อการแยกคู่ของพีก (peak) ซึ่งจะบอกถึงการปรับ resolution จะสัมพันธ์กับการปรับองค์ประกอบของ mobile phase
พจน์ iii คือ การคงอยู่ (retention) ซึ่งจะบอกว่า เมื่อ retention (k) เพิ่ม Rs ก็จะเพิ่มด้วย
เห็นได้ว่า การปรับ resolution สามารถทำได้จากการปรับค่าต่าง ๆ ตามตัวแปรในสมการที่ (1) นั่นเอง |
| |
|
| 3. |
การปรับความแรงของ mobile phase (the role of the solvent in controlling selectivity) |
| |
| |
|
| 3.1 |
การปรับความแรงตัวทำละลาย (solvent strength)
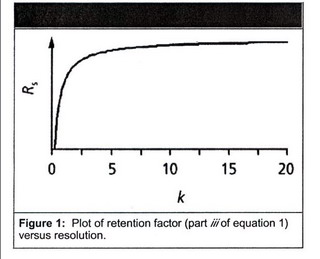
เริ่มต้นการแยกสารด้วยสิ่งที่ทำได้ง่ายที่สุดก่อน นั่นคือ การปรับความแรงของ mobile phase ตามพจน์ iii ของสมการที่ 1 ถ้าสร้างกราฟระหว่าง retention factor กับ resolution จะได้กราฟ ตามรูปที่ 1 นั่นคือ Rs จะดีเมื่อ retention หรือ capacity factor อยู่ในช่วง 2<k<20 ซึ่งในทางปฏิบัติจะค่อย ๆ ลดความแรงของ solvent B (organic solvent) ลงทีละ 10% จาก 90% เป็น 80% และ 70% ตามลำดับ จน retention time ของทุกpeakอยู่ในช่วง 2<k<20 ตามรูปที่ 1 และ 2 |
| |
 |
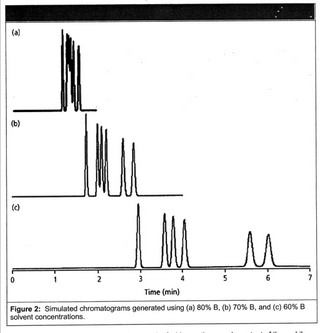 |
รูปที่ 1 และ 2 |
| |
|
| 3.2 |
การปรับละเอียดความเข้มข้นของ solvent B (fine tuning) อีกครั้ง เพื่อให้ได้ Rs > 1.5 ดังรูปที่ 3 |
| |
|
| 3.3 |
การเปลี่ยนชนิดของ mobile phase
การปรับ solvent strength เพียงอย่างเดียวอาจจะแยกสารได้มากมายหลายชนิด แต่สารบางชนิดแม้จะลองปรับความเข้มข้นของ acetonitrile (ACN) ทุกความเข้มข้นแล้ว การแยกชัดก็ยังไม่ดี จะต้องเปลี่ยนชนิดของ mobile phase ตามพจน์ ii ของสมการที่ (1) จาก acetoniltrile (ACN) เป็น MeOH แล้วทำ fine tuning อีกครั้ง แต่ถ้าการแยกชัดยังไม่น่าพอใจอีก ก็ต้องเปลี่ยนชนิดของ mobile phase อีกครั้ง เป็น tetrahydrofuran (THF) |
| |
|
| 3.4 |
การใช้ organic mobile phase สองชนิดผสมกัน (blend solvent)
ถ้าใช้ทั้ง ACN MeOH และ THF แล้วแต่การแยกชัดก็ยังไม่ดี ให้ใช้ solvent ผสมโดยการสังเกตผลการแยกของ mobile phase แต่ละชนิด (ดังรูปที่ 4) |
| |
|
|
| 4. |
การปรับปัจจัยอื่นที่มีผลต่อการแยก (pH, temperature and column type) |
| |
| |
|
| 4.1 |
ความเป็นกรด-เบสของวัฏภาคเคลื่อนที่ (mobile phase pH)
สำหรับตัวอย่างที่สามารถแตกตัวได้ (ionic sample) ที่แนะนำให้ใช้ 0.025 M phosphate buffer pH 2.5 ซึ่งจะช่วยลดการแตกตัวของ acidic compound และ silanol group ของstationary phase ทำให้การเกิดอันตรกิริยา (interaction) ระหว่าง stationary phase กับ acidic และ basic compound น้อยลง การเกิด peak tailing ก็น้อยลงด้วย |
| |
 |
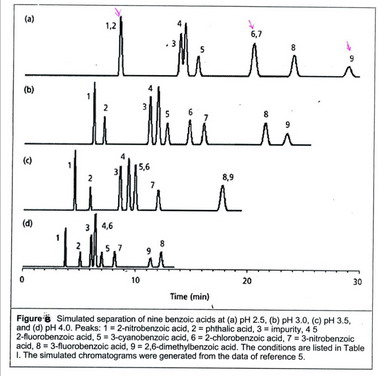 |
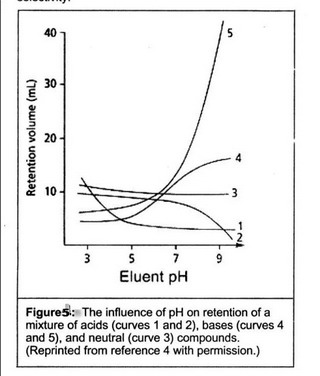
รูปที่ 5 และ 6 |
| |
|
| |
พิจารณาจากรูปที่ 5 จะเห็นว่า เมื่อ pH ของ mobile phase เปลี่ยน เวลาคงอยู่ (retention time) ของ acidic sample (curve 1, 2) และ basic sample (curve 3,4) จะเปลี่ยนอย่างมาก ดังนั้นการปรับ selectivity ของสารประเภทที่แตกตัวได้ โดยการปรับ pH จะมีผลอย่างมาก ซึ่งการปรับ pH ของ mobile phase จะต้องให้ความเข้มข้นของ mobile phase (%B) คงที่ และโดยการค่อย ๆ ปรับ pH เพิ่มทีละ 0.5-1 เพราะการเปลี่ยน pH เพียงเล็กน้อย จะทำให้ทั้ง retention และ ลำดับของpeakเปลี่ยนไปมาก (ดังรูปที่ 6) และระลึกไว้เสมอว่าบัฟเฟอร์ที่ใช้ควรจะมี buffer capacity ที่ดี ซึ่งจะทำให้สภาวะในการแยกมี robustness มาก นั่นคือ บัฟเฟอร์ที่ใช้ควรมี pH อยู่ในช่วง ?1 unit ของค่า pKa ของบัฟเฟอร์ โดย phosphate buffer จะใช้ได้ดีในช่วง pH 2.0–3.1 และ 6.2–8.2 ส่วน acetate buffer จะใช้ได้ดีในช่วง pH 3.8 – 5.8 หรือใช้บัฟเฟอร์ทั้งสองชนิดผสมกันก็จะใช้ได้ตลอดช่วง pH 2–8 |
| |
|
| 4.2 |
อุณหภูมิของคอลัมน์ (column temperature)
โดยทั่วไปการเปลี่ยนแปลงอุณหภูมิของคอลัมน์จะทำให้ retention time เปลี่ยนแปลงไปด้วย ซึ่งจะมีผลต่อ ionic sample มากกว่า neutral sample โดยการเปลี่ยนแปลงอุณหภูมิ 1 oC จะทำให้ retention time ของ ionic sample เปลี่ยนไป 1-3% ดังนั้นการปรับอุณหภูมิจะมีผลต่อ selectivity เพียงเล็กน้อยเท่านั้น แต่เพื่อความ reproducible ของ retention time จึงควรควบคุมอุณหภูมิให้คงที่ |
| |
|
| 4.3 |
การคัดเลือกคอลัมน์ (column selection)
การปรับ selectivity โดยการเปลี่ยนชนิดของคอลัมน์ เป็นวิธีที่ไม่สะดวกนัก และมีราคาแพงกว่าการเปลี่ยนชนิดของ mobile phase ดังนั้นจะใช้วิธีนี้เมื่อการปรับด้วยปัจจัยต่าง ๆ ที่กล่าวมาแล้วก็ยังไม่ทำให้การแยกดีขึ้น ซึ่งการเปลี่ยนชนิดของคอลัมน์คือการเปลี่ยนชนิดของ stationary phase chemistry คือเปลี่ยนจาก C8 หรือ C18 เป็น cyano column และ phenyl column (ดังตัวอย่างในรูปที่ 7) ซึ่งจะมีผลอย่างมากต่อ selectivity และลำดับการถูกชะออกจากคอลัมน์ (peak spacing) ทำให้ไม่สามารถทำนายการเปลี่ยน selectivity จากคอลัมน์หนึ่งไปอีกคอลัมน์หนึ่งได้ |
| |
|
| |
|
|
| 5. |
การเปลี่ยนสมบัติทางกายภาพ (physical properties) ของคอลัมน์ (changing column conditions: flow rate, column size, particles)
แม้ว่าการปรับ selectivity โดยการปรับ mobile phase composition, pH อุณหภูมิ และชนิดของคอลัมน์แล้ว ทำให้การแยกโดยรวมและ peak spacing เป็นที่น่าพอใจ แต่ยังมี peak บางคู่ที่ยังแยกได้ไม่สมบูรณ์ (Rs< 1.5) การปรับพารามิเตอร์ต่าง ๆ ของตัวคอลัมน์ ตามพจน์ i ของสมการ (1) จะช่วยให้การแยกดีขึ้น โดยการปรับอัตราเร็วของ mobile phase ก่อน จากนั้นจึงปรับขนาดของคอลัมน์โดยการเพิ่มความยาวคอลัมน์ และสุดท้ายจึงลดขนาดของ packing material จาก 5 mm เป็น 3 mm แต่การเพิ่มความยาวและลดขนาดของ packing material ลง จะมีผลต่อความดัน และระยะเวลาในการแยก ซึ่งต้องมีการหาค่าเหมาะที่สุด (optimized) เพื่อผลการแยกที่ดีในเวลาอันรวดเร็ว |
| |
|
| 6. |
การเปลี่ยนการแยกสารจาก mobile phase composition คงที่ (isocratic run) มาใช้ gradient run
การแยกสารโดยใช้ gradient run หมายถึง การแยกสารภายใต้เงื่อนไขมาตรฐาน (standardized condition) เพื่อดูองค์ประกอบที่หลากหลายของสารและความยากง่ายในการจะแยกสารนั้น ๆ ได้อย่างรวดเร็ว การใช้ gradient run สำหรับการเริ่มทำ method development มีข้อดีคือ องค์ประกอบของสารทุกชนิดจะถูกชะออกจากคอลัมน์ภายในเวลาที่แน่นอนและภายใต้สภาวะที่มี retention factor ที่เหมาะสม ตาม gradient time ที่กำหนดไว้ โดยที่ไม่จำเป็นต้องทราบข้อมูลขององค์ประกอบเหล่านั้นมาก่อน และประการสำคัญคือ การทำ gradient run ในขั้นตอนของการพัฒนาระเบียบวิธี (method development) เพื่อที่จะทราบข้อมูลว่า สุดท้ายแล้วสารประกอบหรือสารตัวอย่างที่ต้องการจะแยก จำเป็นต้องใช้ isocratic run หรือ gradient run จึงจะทำการแยกได้สำเร็จ
สภาวะเริ่มต้นสำหรับการทำ gradient run เหมือนกับสภาวะเริ่มต้นในขั้นตอนการคัดเลือกคอลัมน์ แต่เปลี่ยน gradient time เป็น 5-100% solvent B ในเวลา 30 นาที และคงที่ที่ 100%B อีก 5 นาที และในการ run แต่ละครั้งเมื่อสิ้นสุดแต่ละ gradient time จะต้องรอให้คอลัมน์ equilibrate ที่สภาวะเริ่มต้น (5%B) อย่างน้อย 10 นาที และเมื่อทดลองแยกองค์ประกอบสารด้วย gradient run ตามตัวอย่างในรูปที่ 8 แล้วลองคำนวณหาว่าควรจะใช้ isocratic run หรือ gradient run ในการแยกสารกลุ่มนี้ วิธีการดังกล่าวนี้เรียกว่าการทำ scouting gradient run |
| |
|
| |
เมื่อให้ |
| |
|
| |
โดย ถ้า |
Dtg /tG > 0.40 ควรจะใช้ gradient run |
| |
Dtg/tG < 0.25 ควรจะใช้ isocratic run |
ถ้า |
Dtg/tG อยู่ในช่วง 0.25 – 0.40 ให้ลองใช้ isocratic run ก่อน ถ้าไม่ได้ผลจึงใช้ gradient run |
|
| |
|
| |
จากผลของการทำ scouting gradient run เราจะนำค่า retention time เฉลี่ยของพีคแรก และพีคสุดท้าย มาเทียบกับ retention time ในตารางที่ 2 เราก็จะทราบว่าต้องใช้ความเข้มข้น ACN เท่าใดสำหรับการทำ isocratic run เช่น retention time เฉลี่ยของพีคแรกและพีคสุดท้ายเท่ากับ 23.5 และเราใช้ความยาวคอลัมน์ 150 มม. ระบบผสมmobile phase แบบ high-pressure mixing ซึ่งมีปริมาตร V0 2.3 mL เราก็จะเลือก %ACN เท่ากับ 65% (อยู่ระหว่าง 60-70%) จากนั้นเราก็ทำ fine-funning หาความเข้มข้นของ mobile phase ที่เหมาะสมได้ทันที ทำให้ลดเวลาที่ต้องปรับ solvent strength ครั้งละ 10% ลงไปได้
ตารางที่ 2 Guidelines for converting a scouting gradient run into isocratic conditions. |
| |
% Acetonitrile |
L (mm) |
150 |
150 |
150 |
75 |
75 |
75 |
V0 (mL) |
0.2 |
2.3 |
4.5 |
0.2 |
2.3 |
4.5 |
0 |
|
|
|
|
|
|
10 |
4 |
6 |
7 |
2 |
4 |
5 |
20 |
7 |
9 |
10 |
4 |
5 |
7 |
30 |
10 |
12 |
13 |
5 |
7 |
8 |
40 |
14 |
15 |
17 |
7 |
8 |
10 |
50 |
17 |
18 |
20 |
8 |
10 |
11 |
60 |
20 |
21 |
23 |
10 |
12 |
13 |
70 |
23 |
25 |
26 |
12 |
13 |
14 |
80 |
26 |
28 |
29 |
13 |
15 |
16 |
90 |
29 |
31 |
32 |
15 |
16 |
18 |
100 |
|
|
|
|
|
|
|
| |
|
| |
โดยสรุป จะสามารถแยกองค์ประกอบของสารด้วยเทคนิค HPLC โดยมีหลักเกณฑ์ในการแยกดังนี้ ทำ scouting gradient run เพื่อดูความเป็นไปได้ที่จะใช้ isocratic run ซึ่งถ้าใช้ isocratic run ได้จะเป็นการดี จากนั้นลองเปลี่ยน % ACN จาก gradient run สู่ isocratic run แล้วปรับ solvent strength เพื่อให้ retention อยู่ในช่วง 2<k<20 จากนั้นจึงปรับ selectivity โดยการปรับ ชนิดของorganic solvent, pH และอัตราเร็วของ mobile phase จากนั้นจึงเพิ่มความยาวคอลัมน์ หรือลดขนาดของ packing material หรือสุดท้ายลองเปลี่ยนชนิดของคอลัมน์ (ตามรูปที่9) |
| |
|
| |
| |
|
| |
รูปที่ 9 ขั้นตอนการพัฒนาวิธีการแยกสารด้วยเทคนิค reverse phase HPLC |
| |
|
|